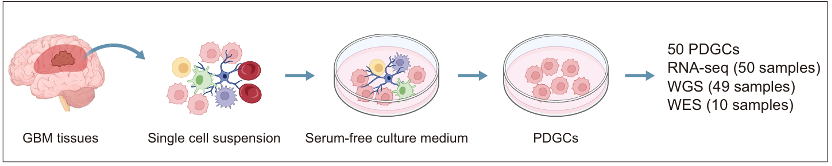
胶质母细胞瘤(GBM)是最常见的脑肿瘤,目前仍无法治愈。GBM原代培养细胞被广泛用于药物筛选和基础研究,但这些细胞缺乏全面的基因组和药理学特征分析。2024年8月8日,北京脑科学与类脑研究所陈坚团队、南京医科大学汪强虎团队、首都医科大学天坛医院张伟团队以及南京医科大学第一附属医院尤永平团队的研究人员合作在Nature Communications上发表了文章Multi-omics and pharmacological characterization of patient-derived glioma cell lines,收集了50株患者来源的胶质瘤细胞(PDGC)系,并进行全面的基因组、转录组和药物应答特征分析,为GBM个体化治疗和药物开发提供了重要依据。

根据50个PDGC的转录组特征,研究人员鉴定出PDGC的三种分子亚型:间质型(MES)、前神经型(PN)和氧化磷酸化型(OXPHOS)。MES亚型富集了上皮-间质转化(EMT)以及免疫相关通路,PN亚型富集了神经元发育相关通路,OXPHOS亚型富集了线粒体相关功能和氧化磷酸化通路。相对于传统的基于肿瘤组织的分型,PDGC分型具有稳定性高、亚型间药物反应差异大的特点。
对配对的PDGC及其亲代肿瘤组织的转录组进行分析发现,60%左右的PDGC维持了亲代肿瘤的亚型特征。通过对PDGC及组织中的肿瘤细胞进行scRNA-seq分析发现,PDGC与组织中的肿瘤细胞在表达模式上具有相似性,且保持了亲代肿瘤的瘤内异质性,但培养后的PDGC中OXPHOS亚型的细胞比例增加。
为了研究三种亚型的差异,研究人员首先利用TCGA的GBM患者临床信息进行生存分析发现,MES亚型的患者预后最差。通过放疗敏感性分析发现,MES亚型细胞呈现放疗抵抗的表型,PN亚型的细胞相对敏感。通过基因组变异分析发现,MES亚型富集PTEN和NF1变异,PN亚型富集ATRX和CDK4变异,OXPHOS亚型富集RB1和MYC/MYCN变异。对三种亚型的细胞进行成瘤测试发现,PN和OXPHOS细胞能在免疫缺陷小鼠颅内稳定成瘤,而MES细胞成瘤率低(2/13)。
接着,研究人员对PDGC进行了药物敏感性分析。开始使用1466个小分子药物在3个PDGC上进行初筛,得到214个具有杀伤潜力的药物,在45个PDGC上进行进一步筛选。药物应答谱分析显示,PN亚型PDGC对酪氨酸激酶抑制剂敏感,而OXPHOS亚型PDGC对组蛋白去乙酰化酶抑制剂、氧化磷酸化抑制剂和HMG-CoA还原酶抑制剂敏感。

研究人员对HMG-CoA还原酶抑制剂(文中使用Lovastatin)的杀伤作用进一步研究。相对于MES和PN亚型,OXPHOS亚型的细胞对Lovastatin更敏感。小鼠体内实验证明,Lovastatin能有效减小皮下肿瘤的大小。对于颅内肿瘤,Lovastatin能抑制肿瘤细胞增殖和增强细胞凋亡。
此外,这一研究也首次发现采用无血清培养基培养PDGC的严重问题。采用无血清培养基培养的PDGC,特别是长期传代的PN和OXPHOS亚型PDGC,大量携带在GBM患者中罕见的MYC/MYCN扩增。无血清培养系统可以激活MYC通路,并发现GBM组织中存在具有MYC扩增的肿瘤细胞,这些肿瘤细胞在无血清培养系统中具有一定的生长优势,并可能最终占据主导地位。该研究为理解原代胶质瘤细胞培养和临床转化提供了宝贵资源,并强调了无血清PDGC培养系统存在不可忽视的问题,为进一步改进和提高这一培养系统提供了基础。
PDGC是研究GBM的重要工具,而MES亚型PDGC成瘤率低,导致大多数体内研究可能主要局限于PN和OXPHOS亚型,单个GBM组织中同时存在多种肿瘤细胞亚型,仅消除PN和OXPHOS亚型的肿瘤细胞无法有效阻止肿瘤发展,这可能是GBM基础研究向临床实践转化的成功率较低的原因之一。
论文信息
南京医科大学与北京脑科学与类脑研究所联合培养博士吴敏为本文第一作者,北京脑科学与类脑研究所陈坚团队的王婷婷、袁然,首都医科大学天坛医院季楠,苏州大学附属第一医院陆挺,南京医科大学汪强虎团队的吴玲祥博士为本文的共同第一作者。
论文链接
https://www.nature.com/articles/s41467-024-51214-y
